之前我们曾探讨过亮蓝分析有杂峰干扰的原因和靛蓝分析回收率不稳定的原因,亮蓝分析有杂峰干扰是因为亮蓝存在3个同分异构体,靛蓝回收率不稳定是因为温度、光照、时间等因素会影响靛蓝溶液的稳定性。
关于合成着色剂的分析我们有一系列的小知识想和大家分享,今天为大家带来的是关于赤藓红分析时回收率不稳定的原因
本文所指的赤藓红,CAS是16423-68-0,我们称之为赤藓红是参考《GB 5009.35-2016 食品安全国家标准 食品中合成着色剂的测定》,在某些文献资料中大家可能会看到将CAS是16423-68-0的物质称之为赤藓红B,主要由于俗称的问题。网上搜索赤藓红,你一定会搜索到两个不同CAS的化合物,还有一个CAS号是568-63-8,通过比较化学式,可以看出这两个化合物互为同分异构体。CAS号是化合物的身份证,是化合物的唯一标示,在合成着色剂分析时受俗称的影响,很容易选错分析对象,建议大家在选购合成着色剂的时候,一定要将CAS号作为唯一标识。
|
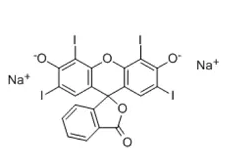
CAS:16423-68-0 |
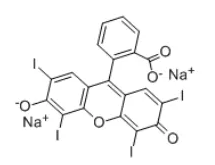
CAS:568-63-8 |
在GB 5009.35中有一种合成着色剂的提取方法:聚酰胺吸附法。在操作的时候很不方便,目前已经有商品化的聚酰胺固相萃取小柱代替,比如安谱实验的CNW Poly-sery PA 聚酰胺小柱,因其操作方便、节省时间、节省试剂、对多种合成着色剂处理后结果准确且回收率高,因而备受广大消费者的青睐,将其用于8种合成着色剂的前处理实验过程和结果如下文所示。
SPE
小柱:CNW Poly-sery PA 聚酰胺小柱 (500mg/6mL)
活化:5mL甲醇
平衡:5mL 水
上样:5mL 1ppm 8种合成着色剂标准品,溶剂柠檬酸溶液(pH 3.0~4.0)
淋洗:5mL 甲醇:甲酸:去离子水(4:2:4)(V/V/V),淋洗后抽干小柱中的溶液
洗脱:3mL*2 10%氨水甲醇
收集洗脱液,并于50℃氮吹至干,用甲醇:0.02M乙酸铵溶液(1:1)定容至1mL,充分溶解后,上机分析。
仪器条件
色谱柱:C18-Wp(4.6mm*250mm,5um)
流动相:A:甲醇B:0.02M乙酸铵
梯度洗脱:0min 15%A,5min 35% A,12~22min 95%A,22.5~30min 15%A
流速:1.0mL/min
柱温:25℃
波长:254nm
进样量:10ul
实验结果
表1 8种合成着色剂实验结果
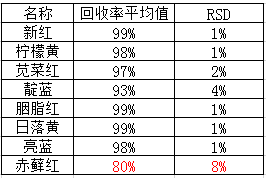
结果表明,除赤藓红之外,其他7种合成着色剂的回收率均大于90%,RSD小于5%,唯独赤藓红回收率较低,且多次实验发现其回收率在70%~90%之间,回收率不稳定。
原因分析
那么到底是什么原因导致赤藓红回收率不稳定呢。仔细阅读国标,可以发现对于含赤藓红的样品,其提取方法采用的是液液——分配法,而非聚酰胺吸附法,但是国标并没有对赤藓红为何不能采用聚酰胺吸附法做解释说明。结合赤藓红的化学结构和GB 5009.35我们来分析一下原因。

液-液分配法原理,加盐酸使赤藓红结构上的Na反应后变为H,赤藓红分子上的酚羟基与三正辛胺分子中的氮原子形成氢键,生成不溶于水的化合物,被萃取到正丁醇中,加饱和硫酸钠去除有机相中残留的水分,正己烷去除油脂类杂质,用氨水做反萃溶剂,加入氨水,使化合物的氢键断裂,赤藓红进入水相,乙酸调pH至中性,浓缩后待测。
聚酰胺吸附法的原理,聚酰胺是由酰胺键聚合形成的高分子化合物,其酰胺基可与羟基酚类、酸类、醌类、硝基等化合物以氢键形式结合而被吸附。其他7种合成着色剂均含有较多的磺酸钠基团,在酸性条件下转变成磺酸根,与聚酰胺的结合很紧密,甲醇-甲酸溶液并不能使其分离,可以作为淋洗溶剂,淋洗掉一些杂质,加水也不能将其分离,同时可以洗去一些水溶性杂质,加入乙醇-氨水-水,将合成着色剂解析出来,乙酸调pH至中性,浓缩后待测。SPE的方法也是利用了此原理,酸性条件上样,使目标物与聚酰胺结合,再用一定比例的甲醇:甲酸:去离子水淋洗去除杂质,然后用氨水甲醇洗脱掉目标物,浓缩复溶待测。所以这7种合成着色剂用聚酰胺粉和聚酰胺小柱均能得到较好的结果。而赤藓红在酸性条件下Na反应后变为H,酚羟基也能与聚酰胺结合而被吸附,但是在甲醇有机相存在的条件下,和聚酰胺的结合并不紧密,容易溶解在甲醇中随着淋洗液流出,导致洗脱回收率低且不稳定。通过设计淋洗和不淋洗步骤进行结果比较,发现不淋洗时赤藓红的回收率大约93%,明显高于淋洗时赤藓红的回收率80%左右。因聚酰胺在用于合成着色剂测定时淋洗可以除掉一些干扰分析的杂质成分,故淋洗步骤很有必要,如果赤藓红和其它合成着色剂同时用聚酰胺小柱分析时,需要关注淋洗溶液和基质的复杂程度,决定是否需要在淋洗液中加入甲醇有机试剂。
除了用聚酰胺小柱测定赤藓红时淋洗溶液不能用甲酸-甲醇溶液外,要使赤藓红的实验结果准确、回收率高还需要注意另外两个方面的问题:
(1)上机之前过滤所用的滤膜不得使用尼龙滤膜,因为尼龙的化学成分就是聚酰胺,会吸附合成着色剂;
(2)建议赤藓红上机溶液的溶剂中加入一定比例的甲醇,如甲醇:水(1:1)或甲醇:0.02M乙酸铵(1:1),而非用纯水做溶剂。因为我们多次实验发现经过氮吹浓缩后,纯水复溶,管壁上会残留很多肉眼可见的赤藓红(红色),经过长时间的超声、涡旋都很难溶解掉,上机分析回收率大约才20%左右,但加入一定比例的甲醇后很容易将赤藓红溶解下来,且甲醇本来也是流动相的一部分,用流动相做溶剂合情合理。